2. Молекулярная физика
 Читать 0 мин.
Читать 0 мин.
2.1. МКТ
Основные положения МКТ:
-
все тела состоят из мельчайших частиц: молекул, атомов или ионов;
-
эти частицы постоянно и хаотически двигаются;
-
между частицами существует взаимодействие: на больших расстояниях они притягиваются, а на маленьких ― отталкиваются.
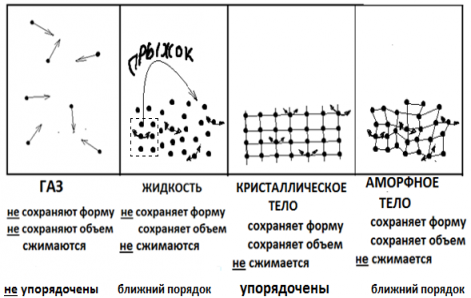
В рамках работы с молекулярно-кинетической теорией необходимо знать и отличать такие понятия, как молекула, атом или ион.
Атом — электронейтральная частица вещества микроскопических размеров и массы. Атом состоит из атомного ядра и электронов. Атомное ядро — центральная часть атома, в которой сосредоточена основная его масса. Ядро заряжено положительно, заряд ядра определяет химический элемент, к которому относят атом. Электроны — стабильные, отрицательно заряженные элементарные частицы, летающие вокруг ядра. (см. Рис. 1).
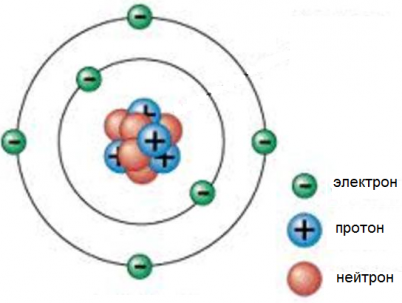
Рис 1.
Атом в целом нейтрален, но потеряв или получив электрон, он становится соответственно положительно или отрицательно заряженным. Такие атомы называются ионами.
Молекула — частица, образованная двумя или большим количеством атомов. Между молекулами может существовать взаимодействие: на близких расстояниях они отталкиваются друг от друга, на дальних ― притягиваются. В классической физике молекулы можно представить как маленькие твёрдые шарики.
Итак, молекула является наименьшей частицей вещества, которая обладает его химическими свойствами. В состав молекулы может входить несколько атомов.
Температура ― величина, определяющая скорость молекул.
-
чем выше температура, тем быстрее двигаются молекулы;
-
чем ниже температура, тем медленней двигаются молекулы.
Внутренняя энергия ― сумма кинетической энергии и энергии взаимодействия молекул.
-
внутренняя энергия увеличивается при повышении температуры и уменьшается при понижении;
-
внутренняя энергия не зависит от движения тела как целого.
Идеальный газ
Идеальный газ ― газ, взаимодействием, между частиц которого можно пренебречь.
Для удобства в физики часто используются математические модели, составленные из идеальных физических объектов.
Модель, используемая при описании газовых процессов, называется идеальный газ.
Идеальный газ — модель газа, в которой в рамках молекулярно-кинетической теории введено несколько условий.
-
взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией;
-
суммарный объём молекул газа пренебрежимо мал;
-
между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги;
-
время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями.
В рамках термодинамики идеальным называется газ, подчиняющийся термическому уравнению состояния Клапейрона-Менделеева и главному уравнению МКТ.
Броуновское движение ― беспорядочное движение частиц твердого вещества в газе или жидкости, вызванное постоянными соударениями с молекулами газа или жидкости.
Диффузия ― взаимное проникновение молекул одного вещества, в область, занимаемую другим веществом.
Свойства диффузии:
-
наблюдается во всех телах (твёрдых, жидких, газообразных);
-
наиболее быстро происходит в газах, медленней в жидкостях и еще медленнее в твёрдых телах;
-
скорость диффузии увеличивается с ростом температуры и уменьшается при её уменьшении.
Конвекция ― явление перемешивания холодного и горячего воздуха, связанное с подъемом более горячего воздуха и опусканием более холодного.
Способы передачи тепла:
-
конвекция (осуществляется преимущественно в жидкости);
-
теплопередача (осуществляется преимущественно в твёрдых телах);
-
лучистый теплообмен.
Температура в Кельвинах = температура в Цельсиях + 273°.
T (K) = T (C) + 273°, где T (K) и T (C) ― это температура в соответствующих шкалах температур.
Основное уравнение МКТ: P = nkT, где
P ― давление газа (Па);
n ― концентрация молекул (1/м3);
k ― постоянная Больцмана, равная 1,38 ∙ 10-23.